سارکوم رحمی
#علائم بیماری سارکوم رحم#در معرض تاموکسیفن#یائسگی#تومورهای درون رحم#هیستراکتومی1403/2/18 8:31:06 PM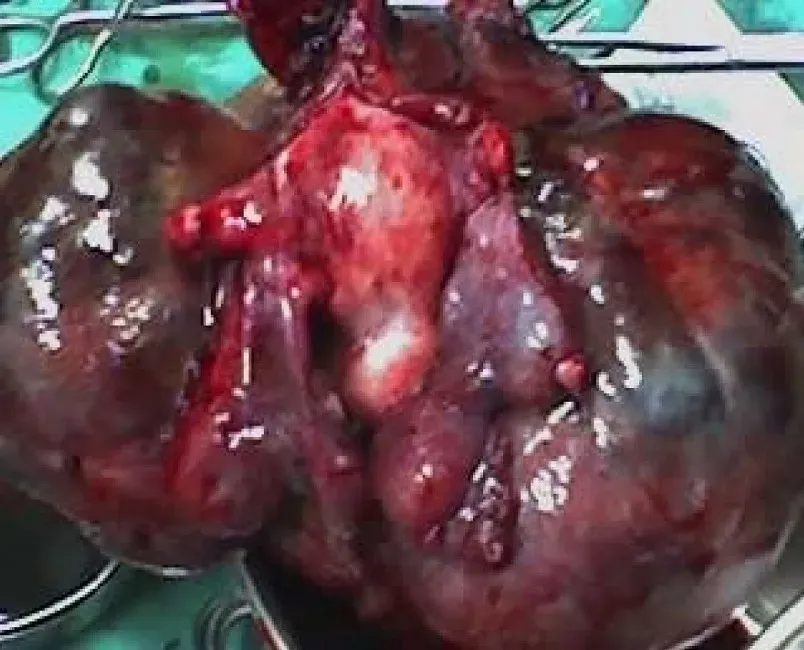
گروهی از سرطان شناسان زنان قصد دارند که یک بررسی اجمالی بر مدیریت لیومیو سارکوم رحم و تخمدان فراهم آوردند . لیومیوسارکوم رحم و تخمدان یک سرطان کم یاب و هجومی است که به تخصص های بخصوصی برای مدیریت بهینه نیاز دارد . سارکوم رحم تقریبا 8% سرطان های رحمی را ، با وقوعی تقریبا U 0.4 در هر 100000 زن ، نشان می دهد . لیومیوسارکوم ها ( LMSs) معمول ترین زیر گروه می باشند ، بیشتر آنها سرطان های درجه بالا و با خطر زیاد برای بازگشت مجدد و پیشرفت آن می باشد . بقای کلی به مرحله آن وابسته می باشد ، تخمین زده می شود که در مرحله یک با 5 سال دوام 76 % ، در مرحله دو 60% ، مرحله سه 45% و در مرحله چهارم بیماری 29 % امکان بقای کلی وجود دارد . لیومیوسارکوم رحمی با کمک فدراسیون بین المللی زنان و زایمان 2009 که سیستم مرحله بندی سارکوم رحمی را داشتند مرحله بندی شده است ، اگر چه که سیستم های مرحله بندی آناتومیک در پیش بینی بقا و دوام ضعیف عمل می کنند. فاکتور های دیگری که برای پیش بینی اثرات ذاتی ارزیابی شده است شامل : مورسلاتوری تومور ، شاخص میتوزی و درجه تومور می باشد . یک نوموگرام که شامل فاکتور های پیش بینی غیر آناتومیک اضافی مانند : سن بیمار ، درجه تومور و نرخ میتوزی می باشد تخمین های بهتری از بقای کلی را فراهم می کند . (سیارک)
اپیدمیولوژی
بیشتر بیماران دارای LMS رحمی هیچ گونه عوامل شناسایی خطر را ندارند . بیمارانی که جهش ژنی P53 دارند ( سندروم Li Fraumeni ) در مقابل انواع سرطان ها خطر بیشتری برای سارکوم بافت نرم که شامل : LMS رحمی می باشد، دارند. بیماران با جهش Rb که از رتینوبلاستوما دوران کودکی نجات پیدا کردند ، و نجات یافتگان رابدومیوسارکما (rhabdomyosar-coma ) کودکی و یا هر گونه سرطان های دوران کودکی دیگر ، که از درمانی شامل تابش استفاده کرده اند ، خطر زیادتری برای سرطان های ثانویه شامل : LMS رحمی دارند . سندروم خانوادگی لیومیوماتوزیس ارثی با کارسینوم سلول کلیوی ( HLRCC ) ، که در آن جوانه جهش فیومارات هیدراتاس وجود دارد ، با یک خطر افزایش یافته ای برای LMS رحمی مرتبط شده است . برخی از مطالعات خطر بالاتری برای سارکوم رحمی در میان زنان با یک سابقه چاقی و دیابت و همچنین در میان زنانی که در معرض تاموکسیفن قرار دارند پیشنهاد داده است .
پاتولوژی (آسیب شناسی)
ضوابط استندفرد معمولا برای تشخیص LMS رحم استفاده می گردد، بافت شناسی ترکیبی، سلول مردگی تومور و نرخ میتوزی. اجماع ناکاملی در رابطه با طبقه بندی LMSs رحم وجود دارد. ایمونوهیستوشیمی برای نشانگر تفکیک ماهیچه نرم مانند اکتین ماهیچه نرم و کالدسمان می تواند برای کمک به تشخیص استفاده شود. بافت شناسی انواع LMS رحم مانند LMS اپیتلیویید و میکسوید ممکن است ضوابط متفاوتی داشته باشد. به جهت اختلاف های اندک تشخیص بافت شناسی LMS رحم، بررسی کارشناسی توسط پاتولوژیست های بافت شناسی و/یا پاتولوژیست های سارکوم توصیه می شود.(سیارک)
بیولوژی مولکولی و ژنتیک
هیچ دگرگونی منفردی در LMS رحم شناسایی نشده است. اکثر تومورها وضعیت غیر عادی کروموزمی چندگانه از خود نشان می دهند. شرایط ژنتیکی در LMS قابل تحقیق می باشد. اما می تواند اهداف درمان را مشخص کند. 16، 17 پروفایل ژنتیکی می تواند با شناسایی امضا ژن که بین تومور LMS تنبل رحم و تومور پیش رونده بالینی تفاوت ایجاد می کمند، پیش بینی درمان را تقویت کند.
تشخیص بیماری
علائم بیماری شامل درد یا فشار لگنی ، یا خونریزی غیر طبیعی واژینال است. توموگرافی محاسبه شده (سی تی اسکن (CT) ) ، یا عکس برداری بزرگ شده مغناطیسی (MRI) ممکن است جرم رحمی ای را نشان دهد. هیچ عکس برداری ای به تنهایی نمی تواند تشخیص قابل اعتمادی از خوش خیم بودن تومور رحم و یا بدخیم بودن آن ارائه دهد. مطالعه اولیه MRI قبل از عمل بیمار دارای نئوپلاسم مزانشیمال رحمی، دقت کمی در نشان دادن لیومیوم های با مشخصات غیر نرمال از نئوپلاسم مزانشیمال بدخیم دارد. یک مطالعه جداگانه (19 بیمار با ضایعات مزانشیمال رحمی، که سه تا از آن ها LMS بودند) پیشنهاد می دهد که ممکن است MRI قادر به تشخیص بیماری خوش خیم از بدخیم باشد. تومورهای درون رحمی که بزرگ شدن آن ها بعد از یائسگی هم ادامه دارد، سوظن بدخیم بودن را بالاتر می برد. در بیشتر بیمارها ، تشخیص بیماری LMS رحمی در زمان میومکتومی یا هیسترکتومی و با فرض خوش خیم بودن بیماری انجام می گیرد.
مراحل پیشرفت بیماری در جدول زیر آمده است.
|
مرحله |
تعریف |
|
I |
تومور محدود شده با رحم |
|
IA |
e5 cm |
|
IB |
95 cm |
|
II |
تومور تا پشت رحم در لگن گسترش یافته |
|
IIA |
شامل آدنکسال |
|
IIB |
دیگر بافت های لگن را شامل شده |
|
III |
تومور به بافت های شکمی حمله کرده (نه فقط بیرون زده در شکم) |
|
IIIA |
یک طرف |
|
IIIB |
بیشتر از یک طرف |
|
IIIC |
متاستاز سرطان در لگن یا گره های لنفاوی پارا ائورتی |
|
IV IVA |
تومور به مثانه و مقعد حمله کرده |
|
IVB |
فاصله متاستاز |
مرحله بندی
ساراکوم رحم بر اساس سیستم مرحله گذاری فدراسیون بین المللی ژینکولوژی و زنان 2009 مرحله بندی شده است. (جدول بالا)
درمان اولیه / عمل
برای بیمارانی که بیماری آنها به رحم محدود شده است، هیستراکتومی پیشنهاد می شود. اگر سوظنی به بدخیم قبل از عمل باشد، ما مرسلاتوری برعکس را پیشنهاد می کنیم، زیرا سرطان قبل از عمل د ربافت های بدخیم پخش شده است. مرسلاتوری تومور های بدخیم با نتایج حیاتی ضعیفی همراه هستند.
کالبدشکافی گره های لنفافی معمولی ، به طور کلی نیاز نیستند، اما توصیه می شود هنگامی که در گره های لنفافی بزرگ شدگی دیده شود و سوظن بدخیمی داشته باشیم، حتما برداشته شوند. سالپینگو افورکتومی دو طرفه (Bilateral salpingo-oophorectomy (BSO)) برای زنان پیش یائسه و پس یائسه منطقی است، اگرچه اطلاعاتی از بهبود علائم حیاتی در افورکتومی دیده نشده است. گیرنده استروژن و یا گیرنده پروژستورن، در 40% تا 70% رحم های دارای LMS، مثبت گزارش شده است. و اهمیت پیش آگهی ، پیشنهاد می کند که حتی برای زنان پیش یائسه ممکن است افورکتومی منطقی باشد. در هر حال داده های گذشته تفوت بقایی در زنان جوانتر از 50 سال با بیماری رحمی محدود که BSO را انجام داده اند و یا نداده اند، نشان نمی دهد.(سیارک)
برای بیماری های که پیشرفت محلی را نشان می دهند اما هنوز امکان برداشت کامل وجود دارد، تلاش برای برداشتن کل بیماری منطقی است. آمار گذشته نشان می دهد که مقدار زنده ماندن در بین زنان بیماری که بصورت کامل در آن ها برداشته شده بیشتر از زنانی است که مقداری از تومور در انتهای عمل برداشت در آن ها باقیمانده است.
در زنانی که با متاستیک در چند محل مواجه هستند و تومر آنها غیر قابل برداشت است، یک قانون کلی برای هیسترکتومی وجود ندارد. محل هیسترکتومی به بیمار با بیماری متاستاتیک بستگی دارد که کنترل کمی روی خونریزی رحمی دارد.(سیارک)
اپیدمیولوژی
ارزیابی دوباره لاپاروسکوپی لگن خاصره بعد از انجام هیسترکتومی مرسلاتوری باید مورد توجه قرار بگیرد تا هیچ بافت بدخیم باقیمانده ای وجود نداشته باشد. اگر هنوز برداشت گردنه و توجه BSO انجام نشده، برای بیمار منطقی است که فقط هیسترکتومی ساپسرویکال صورت بگیرد.
مدیریت موردی رحم با بیماری محدود
اگرچه خطر عود دوباره بعد از برداشت رحم محدود شده با درجه بالای LMS بیشتر از 50 درصد است اما هیچ دخالت و عمل مشخصی منجر به بهبود زنده ماندن بدون پیشرفت (PFS) یا بهبود علائم کلی حیاتی نشده است. مدیریت استاندارد بعد از برداشت کامل رحم با بیماری محدود مشاهده و نگاه کردن است. نزدیک یک سوم بیمارانی که در زمان هیسترکتومی، فهمیدند که LMS رحمی دارند، در عکس های موردی بیماری متاستاتیک را نشان می دهند. بنابراین CT و یا PET/CT ویا MRI برای جلوگیری از متاستاز توصیه می شود. عکس برداری توموگرافی با نشر پوزیترون (PET) نسبت به CT یا MRI برتری در تشخیص بازگشت بیماری ندارد. عکس برداری PET ممکن است متاستاتیک های با حجم کم را نشان ندهد.
رادیشن (تابش) معین لگن می تواند در ارزیابی ، سعی های احتمالی آینده برای زنان با رحم کارسینو سارکوم، LMS، یا استرما آندومتر سارکوم استفاده شود. علائم حیاتی با تابش معین بهبود نمی یابد. در میان بیماران با LMS رحمی، تفاوتی در نرخ بازگشت محلی در بیمارانی که با رادیشن لگنی معین درمان شده اند و آن هایی که فقط تحت مشاهده و مراقبت بوده اند دیده نمی شود. تلاش های آینده احتمالی از مشاهده دوکسوروبیسینوسوس (doxo-rubicinversus) معین برای بیماران با LMS رحم و کارسینو سارکوم ، مزیتی حیاتی برای دوکسوروبیسین نشان نداده است. مطالعات فاز دو آینده ، از gemcitabine-docetaxel معین، که با دوکسوروبیسین دنبال می شود، نرخ PSF دوساله 78% را نشان داده است. اما در سه سال فقط 58% بدون پیشرفت باقیمانده اند. (سیارک)
اپیدمیولوژی
یک مطالعه کوچک بر روی 81بیمار با تنوع بافت و مرحله سارکوم افوتراین (ofuterine) (مرحله I ، 52 بیمار، مرحله II، 16 بیمار ، مرحله III، 13بیمار ، 53 LMS ، 9 سارکومی بدون تفاوت، و 19 کارسینو سارکوم) با دوکسوروبیسین به علاوه ifosfamide به علاوه سیس پلاتین که با رادیشن دننبال شده اند، بهتر از رادیشن تنها برای مدت 3 سال برای بقای بدون بیماری (55% تا 41%) بوده است، اما نه برای تمام بیماران.(سیارک)
این اطلاعات نمی توانند به حمایت از توصیه ای برای یک شیمی درمانی معین به عنوان یک درمان استاندارد داده شده برای انواع تومورهای ناهمگون و مراحل آنها و حجم نمونه بسیار کوچک آنها و بدون مزیت بقای کلی استفاده شوند . یک مشاهده فاز سه تصادفی بین المللی در مقابل شیمی درمانی کمکی برای 4 سیکل و بعد از آن برای چهار دوره در جریان است .
برای بیماران مبتلا به طور موضعی پیشرفته، LMS رحم به طور کامل برداشته شده، هیچ داده آینده نگری که براساس توصیه های های مدیریت باشد وجود ندارد. انتخاب ممکن است شامل مشاهده، تابش کمکی، انسداد هورمون کمکی، و یا شیمی درمانی کمکی باشد. محل بیماری، درجه بافت شناسی، گیرنده استروژن (ER) و وضعیت پروژسترون (PR) ، اولویتهای بیماران، عملکرد عضو، و بیماریهای همراه می تواند در تصمیم گنجانیده شود. ادامه در پست بعدی....
ترجمه itrans.ir